Lungenembolie: Diagnose und Therapiemöglichkeiten
Einleitung
Die Lungenembolie ist nach wie vor eine gefürchtete Erkrankung, die mit einer hohen Morbidität und Mortalität einhergeht. Eine frühzeitige Diagnose und rasche Einleitung der Therapie ist deshalb wichtig. Die Symptome der Lungenembolie sind wegweisend, können aber auch fehlen und die richtige Diagnose wird oft verpasst [1-7]. Die typischen Symptome sind:
1. Akute Dyspnoe
2. Pleuritischer Schmerz und/oder Pleurareiben
3. Thoraxschmerz, häufig nicht retrosternal
4. Hypoxämie (02-Sättigung < 90%)
5. Hämoptyse
6. Synkope
7. Geschwollene Beine oder Schmerzen
Neben der typischen Symptomatik spielt die Anamnese eine wichtige Rolle. Risikofaktoren für eine akute Lungenembolie sind:
1. Chirurgie oder Beinfraktur während den letzten 3 Monaten
2. Verlängerte Bettruhe (> 3 Tage)
3. Anamnese von Thromboembolie
4. Hereditäre Thrombophilie
5. Malignom
Als einfaches Schema zur Abschätzung der klinischen Wahrscheinlichkeit einer Lungenembolie hat sich das Schema in Abbildung 1 bewährt.
Abbildung 1: Klinische Wahrscheinlichkeit für LE
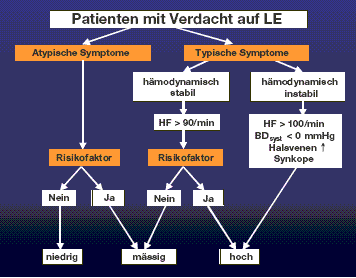
Legende: Die Abschätzung der klinischen Wahrscheinlichkeit einer Lungenembolie ist ein wichtiger Baustein in der Lungenemboliediagnostik, da die zur Verfügung stehenden bildgebenden Verfahren nicht absolut zuverlässig sind. Wells und Kollegen (2) konnten zeigen, dass bei Patienten mit einer geringen klinischen Wahrscheinlichkeit die Diagnose nur in 3.4%, bei Patienten mit einer mässigen klinischen Wahrscheinlichkeit in 27.8% und bei hoher klinischer Wahrscheinlichkeit in 78.4% bestätigt werden konnte. Bei Vorliegen von atypischen Symptomen und fehlenden Risikofaktoren ist die Wahrscheinlichkeit für eine Lungenembolie gering. Bei Patienten mit typischen Symptomen und stabiler Hämodynamik, aber Vorliegen von Risikofaktoren ist die Wahrscheinlichkeit hoch. Bei fehlenden Risikofaktoren ist hingegen die Wahrscheinlichkeit mässig. Bei Patienten mit typischen Symptomen und hämodynamischer Instabilität ist die klinische Wahrscheinlichkeit für eine Lungenembolie immer hoch.
Diagnose der akuten Lungenembolie
Bei Verdacht auf Lungenembolie wird notfallmässig das D-Dimer und gleichzeitig die Sauerstoffsättigung (Biox) bestimmt. Ist das D-Dimer ≤ 500 µg/l und die klinische Wahrscheinlichkeit für eine Lungenembolie gering [5,6], so kann mit hoher Wahrscheinlichkeit eine Lungenembolie ausgeschlossen werden (s. Abbildung 2).
Sind die D-Dimere normal, aber die klinische Wahrscheinlichkeit für Lungenembolie hoch, soll ein Spiral-CT durchgeführt werden, welches mit einer hohen Sensitivität und Spezifität das Vorliegen oder Fehlen einer Lungenembolie bestätigt [7,8]. Bei positivem Spiral-CT ist die Diagnose eindeutig, bei negativem Spiral-CT und hoher klinischer Wahrscheinlichkeit wird eine Pulmonalisangiographie empfohlen [9], welche mit hoher Spezifität den Nachweis einer Lungenembolie erlaubt (s. Abbildung 2).
Abbildung 2: Diagnose der akuten Lungenembolie
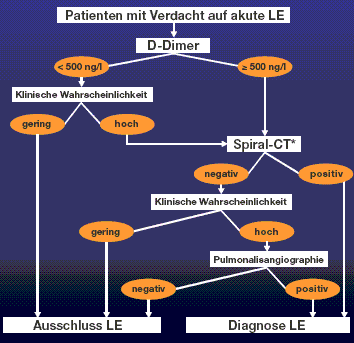
Legende: Aufgrund der hohen Sensitivität der D-Dimere von 98% (ELISA, VIDAS) kann bei ca. 30% aller Notfallpatienten mit Verdacht auf Lungenembolien die Diagnose bei normalem D-Dimer ohne weitere Abklärungen sicher ausgeschlossen werden [5,6]. Gemäss Abb. 2 ist eine weitere Abklärung nur bei Vorliegen von hoher klinischer Wahrscheinlichkeit indiziert. Bei Verdacht auf Lungenembolien und einem D-Dimer ≥ 500 µg/l sind aufgrund der geringen Spezifität der D-Dimere weitere Abklärungen bei allen Patienten durchzuführen.
Die wichtigsten diagnostischen Verfahren (Spiral-Computertomographie, Echokardio-graphie und Pulmonalisangiographie) haben verschiedene Vor- und Nachteile:
Spiral-Computertomographie (CT): Trotz widersprüchlicher Daten hinsichtlich der Sensitivität des Spiral-CT hat sich dieses Verfahren als klinischer Standard in der Lungenemboliediagnostik durchgesetzt [7,8]. Das Spiral-CT weist eine sehr hohe Spezifität auf, ausserdem ist es in der Differentialdiagnose von Thoraxpathologien von grosser Bedeutung (Aortendissektion, Pneumonie, intrathorakaler Tumor, Perikard- und Pleuraerkrankungen). Zudem ist diese Untersuchung praktisch jederzeit verfügbar (24-Stunden-Service). Bei Patienten mit hoher klinischer Wahrscheinlichkeit für Lungenembolie und einem negativen Spiral-CT sind jedoch weitere Abklärungen indiziert. Hingegen ist die Diagnose Lungenembolie bei negativem Spiral-CT und geringer klinischer Wahrscheinlichkeit für Lungenembolie sicher auszuschliessen.
Echokardiographie: Die Echokardiographie ist eine zuverlässige Untersuchung bei hämodynamisch komprimittierten Patienten, d.h. Sensitivität und Spezifität hinsichtlich Lungenemboliediagnostik liegen bei Nachweis einer akuten Druckbelastung des rechten Ventrikels in > 90% vor [3,4]. Aus diesem Grund kann bei einem hämodynamisch instabilen Patienten und einer normalen rechtsventrikulären Funktion und rechtsventrikulären Dimension die Diagnose einer hämodynamisch relevanten Lungenembolie ausgeschlossen werden. Bei Nachweis einer akuten Druckbelastung des rechten Ventrikels (Dilatation, Dysfunktion), hohem systolischem Pulmonalarteriendruck, regionalen Wandbewegungsstörungen des rechten Ventrikels [10] kann die Diagnose spezifisch gestellt werden, so dass bei vitaler Gefährdung zu diesem Zeitpunkt die Triage Lyse vs. Kathetertherapie vs. chirurgische Embolektomie direkt festgelegt werden kann.
Pulmonalisangiographie: Prinzipiell ist diese Technik der gold standard in der Lungenemboliediagnostik mit der höchsten Sensitivität und Spezifität. Die mit dieser Technik verbundene Mortalität ist gering (0.5%) aber nicht zu vernachlässigen [9]. Ausserdem hängt die Qualität der Untersuchung von der Erfahrung des Untersuchers ab. Insgesamt wird die diagnostische Pulmonalisangiographie in der Routine nur noch bei wenigen Patienten mit Verdacht auf Lungenembolie eingesetzt. Aus diesem Grund ist diese Untersuchung das letzte Glied in unserem Fluss-Schema und bleibt den Patienten mit hoher klinischer Wahrscheinlichkeit (ohne Alternativdiagnose) sowie vorhergehend negativen oder inkonklusiven Untersuchungsresultaten vorbehalten.
D
ie Ventilations- und Perfusionsszintigraphie spielt heute eine geringere Rolle in der Diagnostik der Lungenembolie [7]. Diese Untersuchungstechnik ist ein gut etabliertes Verfahren bei Patienten mit Verdacht auf rezidivierende bzw. chronische Lungenembolien. Hingegen ist dieses Verfahren bei Patienten mit akuter Lungenembolie wenig geeignet und wird nur noch bei stark eingeschränkter Nierenfunktion oder Unverträglichkeit auf Röntgenkontrastmittel eingesetzt.
Therapie der Lungenembolie
Die Therapie der akuten Lungenembolie ist abhängig von der Gefährdung des Patienten (s. Abbildung 3). Diese kann aufgrund des Blutdrucks, der Herzfrequenz, der Pulsoxymetrie, der Atemfrequenz und der Halsvenen abgeschätzt werden. Als Mass für die hämodynamische Gefährdung hat sich der Schock-Index etabliert (Quotient aus Herzfrequenz und systolischem Blutdruck), der als negativ bezeichnet wird, wenn er < 1 und als positiv, wenn er ≥ 1 ist.
Keine vitale Gefährdung liegt vor bei Schock-Index unter 1, bei Sauerstoffsättigung > 90% und bei einer Atemfrequenz < 20/Min. Eine vitale Gefährdung liegt vor bei Schock-Index ≥ 1, bei einer Sauerstoffsättigung < 90% und bei einer Atemfrequenz > 20/Min. (Ruhedyspnoe).
Bei allen Patienten soll sofort ein EKG geschrieben und ein venöser Zugang gelegt werden. Neben CK, Troponin, Natrium, Kalium, Kreatinin, CRP, Hämoglobin, Leukozyten und Thrombozyten sollen D-Dimere und BNP bestimmt werden.
Ein Röntgen-Thorax ist fakultativ, die Blutgase sollen in der Regel bestimmt werden. Bei mässigem bis hohem Verdacht soll sofort ein Heparinbolus von 5000 Einheiten i.v. verarbreicht werden sowie nasale Sauerstoffgabe je nach Pulsoxymetrie oder Blutgaswerten.
Bei Vorliegen einer vitalen Gefährdung soll sofort mit der Intensivbehandlung begonnen, bei Schockzustand oder elektromechanischer Dissoziation unverzüglich eine kardio-pulmonale Reanimation eingeleitet werden. Ausserdem sollte notfallmässig eine transthorakale Echokardiographie durchgeführt werden.
Bei Fehlen der rechtsventrikulären Dysfunktion kann eine relevante Lungenembolie ausgeschlossen werden, bei Vorliegen einer rechtsventrikulären Dysfunktion besteht der hochgradige Verdacht auf Lungenembolie.
Abbildung 3: Therapie der akuten Lungenembolie. Vergrössern: darauf klicken.
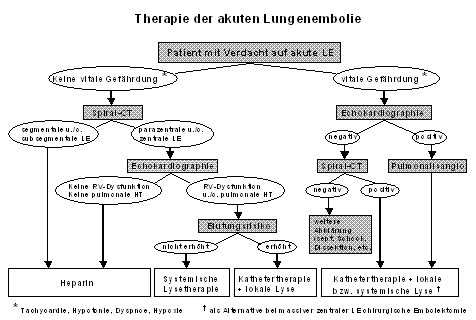
Die Therapie der akuten Lungenembolie (s. Abbildung 3) wird je nach Gefährdung des Patienten durchgeführt. Besteht keine vitale Gefährdung und zeigt das Spiral-CT lediglich segmentale Lungenembolien, und in der Echokardiographie besteht keine RV-Dysfunktion ist eine Behandlung mit Heparin indiziert. Besteht allerdings eine deutliche rechtsventrikuläre Dysfunktion bei normalem Blutungsrisiko (keine Operation innerhalb der letzten 3 Wochen bzw. orale Antikoagulation) ist die systemische Lysetherapie indiziert. Bei erhöhtem Blutungsrisiko ist eine Katheterintervention mit lokaler Lyse angezeigt.
Bei vitaler Gefährdung des Patienten mit positivem Schockindex soll auf das Spiral-CT verzichtet werden und notfallmässig eine Echokardiographie durchgeführt werden. Ist diese negativ, soll ein Spiral-CT nachgeholt werden und bei negativem Befund weitere Abklärungen in Bezug auf septischen Schock, Aortendissektion, etc. eingeleitet werden. Bei positivem Spiral-CT ist die Lysetherapie indiziert [11,12]. Bei positiver Echokardiographie mit den Zeichen der pulmonalen Drucksteigerung und der rechtsventrikulären Dysfunktion soll sofort eine Pulmonalisangiographie und eine Kathetertherapie mit lokaler Lyse durchgeführt werden.
Thrombolyseprotokoll: Bei submassiver und massiver Lungenembolie soll noch am gleichen Tag eine Thrombolyse durchgeführt werden, sofern nicht eine absolute Kontraindikation (aktive Blutung oder Anamnese einer interzerebralen Blutung) besteht. Bei relativen Kontraindikationen (grösserer chirurgischer Eingriff in den letzten 2 Wochen oder ischämischer zerebrovaskulärer Insult in den letzten 2 Monaten, etc.) kann eine Thrombolyse durchgeführt werden, wobei heute z.B. Alteplase 15 mg Bolus i.v. gefolgt von 85 mg während 2 Stunden empfohlen wird (front loaded Schema). Bei Gewicht < 65 kg soll die Dosis reduziert werden. Neben der Thrombolyse soll Heparin mit einer Dosis von 1'000 Einheiten pro Stunde begonnen werden und je nach Gerinnungszeiten 6-stündlich angepasst werden.
Kathetertherapie: Heute bestehen mehrere Möglichkeiten zur Fragmentation oder Entfernung von massiven Lungenembolien mittels Kathetertherapie [13-16]. Die Katheterfragmentation beruht auf einer Verkleinerung des Thrombus durch Rotation eines Pigtail-Katheters oder wiederholtes Aufblasen eines Ballonkatheters [13,14].
Neuere Kathetersysteme erlauben die Zerstörung des Thrombus mittels mechanischer Verkleinerung und Absaugen des Thrombusmaterials [16] Erste Versuche beim Schwein zeigten eine erfolgreiche Zerkleinerung und Absaugung des Thrombusmaterials, gefolgt von einer raschen hämodynamischen Erholung (Aspirex-Katheter; Straub Medical, Wangs, Schweiz). Solche Systeme werden in Zukunft die interventionelle Behandlung vom Patienten mit submassiver oder massiver Lungenembolie erlauben.
Prof. Dr. Otto M. Hess, Klinik und Poliklinik für Kardiologie, Departement Herz und Gefässe, Universitätsklinik Inselspital, Bern.
Referenzen
1. Kucher N, Luder CM, Doemhofer T, et al. Novel management strategy for patients with suspected pulmonary embolism. Eur Heart J 2003; 24:366-76.
2. Wells PS, Ginsberg JS, Anderson DR, et al. Use of a clinical model for safe management of patients with suspected pulmonary embolism. Ann Intern Med 1998; 129:997-1005.
3. Konstantinidis S, Geibel A, Olschewski M, et al. Association between thrombolytic treatment and the prognosis of hemodynamically stable patients with major pulmonary embolism. Circulation 1997; 96:882-8.
4. Goldhaber SZ, Haire WD, Feldstein ML, et al. Alteplase versus heparin in acute pulmonary embolism: randomised trial assessing right-ventricular function and pulmonary perfusion. Lancet 1993; 341:507-11.
5. Kucher N, Windecker S, Banz Y, Schmitz-Rode T, Mettler D, Meier B, Hess OM. Percutaneous catheter thrombectomy device for acute pulmonary embolism: In vitro and in vivo testing. Radiology 2005; 10:852-8.
| Medizin Spektrum |
| |
| 26.9.2005 - ssc |
| |
 |
|